Atomistique et Liaison chimique - PowerPoint PPT Presentation
Title:
Atomistique et Liaison chimique
Description:
Si la dur e de l'exp rience est courte : les franges disparaissent Corpusculaire. Si la dur e de l'exp rience est longue : les franges r apparaissent Ondulatoire ... – PowerPoint PPT presentation
Number of Views:1451
Avg rating:3.0/5.0
Title: Atomistique et Liaison chimique
1
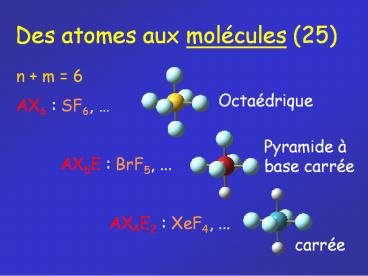
Des atomes aux molécules (25)
n m 6 AX6 SF6, AX5E BrF5,
... AX4E2 XeF4, ...
Octaédrique
Pyramide à base carrée
carrée
2
Des atomes aux molécules (26)
n m 7 AX7 IF7,
Bipyramide à base pentagonale
3
Des atomes aux molécules (27)
- Subtilités
- répulsion n-n gt n-l gt l-l
(n paire libre l paire liée)
4
Des atomes aux molécules (28)
Influence de la mésomérie. Exercice à laide
des modèles de Lewis et VSEPR, expliquer pourquoi
langle H-N-H vaut 113,2 dans laniline, alors
qu il vaut 107,3 dans NH3 et 120 dans lion
iminium (H2CNH2).
Aniline
5
Des atomes aux molécules (29)
- Limites du modèle VSEPR.
- Pourquoi SiH3 est pyramidal et CH3 plan ?
- Pourquoi CaF2 est coudé ?
- Pourquoi C2H4 est plan ?
- Pourquoi BH2 est linéaire ou coudé suivant quil
est irradié par la lumière ? - ...
6
Liens Web
VSEPR http//neon.chem.ox.ac.uk/vrchemistry/ vs
epr/intro/vsepr_splash.html
7
Des atomes aux molécules (30)
- Moments dipolaires électriques.
- Grandeur vectorielle qui na de sens que pour les
systèmes électriquement neutres. - Si le barycentre des charges positives, chargé
q, ne correspond pas au barycentre des charges
négatives, chargé ?q, la norme du moment
dipolaire est égale au produit de la charge q par
la distance d entre les barycentres.
8
Des atomes aux molécules (31)
q en coulomb (C) d en mètre (m) m en C.m ou en
Debye (D) 1 D 3,3.10?30 C.m
Les atomes isolés nont pas de moment
dipolaire. Les molécules diatomiques
homonucléaires non plus. Les molécules
diatomiques hétéronucléaires ont un moment
dipolaire non nul.
9
Des atomes aux molécules (32)
- Latome le plus électronégatif a un excès
délectrons (charge électrique ?q) - q 0 ? liaison purement covalente
- q ? 0 ? liaison polaire
- q n.e ? liaison purement ionique
10
Des atomes aux molécules (33)
Pourcentage dionicité
11
Des atomes aux molécules (34)
Molécules polyatomiques ou en simplifiant
le moment dipolaire moléculaire est égal à la
somme vectorielle des moments dipolaires de
liaison. ? attention à la symétrie !
12
Des atomes aux molécules (35)
Influence de la mésomérie.
mexp très faible et orienté de C vers O
Règle en général mésomérie gt induction
13
Dualité onde-corpuscule (1)
- La lumière selon Newton XVIIe
- vue comme un jet de particules qui rebondissent
sur les miroirs - La lumière selon Maxwell XIXe
- nature ondulatoire qui explique les figures
dinterférences(diffraction, ) - Unification de loptique, de lélectricité et du
magnétisme!
14
Dualité onde-corpuscule (2)
- La lumière selon Einstein XXe
- composée de grains dénergie (photons)
- E hn p h/l
- Effet photoélectrique
- pas démission en deçà de nseuil ? intensité
- Ecinétique f(n) mais pas de I
15
Dualité onde-corpuscule (3)
- Expérience des fentes dYoung
I1
Source
Ecran
Fente
16
Dualité onde-corpuscule (3)
- Expérience des fentes dYoung
Source
I2
Ecran
Fente
17
Dualité onde-corpuscule (3)
- Expérience des fentes dYoung
I1 I2
?
Source
Ecran
Fente
18
Dualité onde-corpuscule (3)
- Expérience des fentes dYoung
I obserbée
Source
Ecran
Fente
19
Dualité onde-corpuscule (4)
- Que ce passe t-il si on diminue lintensité du
rayonnement (envoyer les photons un par un) ? - Hyp 1 corpusculaire
- linterférence ne peut être due quaux
interactions entre 2 photons qui passent par les
deux fentes en même temps! - Elle devrait donc disparaître.
20
Dualité onde-corpuscule (5)
- Hyp 2 ondulatoire
- en diminuant lintensité du rayonnement, la
figure de frange doit être atténuée mais
conservée.
Résultats ni lune ni lautre !
21
Dualité onde-corpuscule (6)
Si la durée de lexpérience est courte les
franges disparaissent ? Corpusculaire Si la
durée de lexpérience est longue les franges
réapparaissent ? Ondulatoire
22
Dualité onde-corpuscule (7)
- Hyp 3 le photon interfère avec lui même en
passant par les 2 fentes !?
Si deux détecteurs derrière les fentes ? les
photons passent soit par lune soit par lautre
fente. Si un seul détecteur ? plus de frange
! La mesure perturbe le système !
23
Dualité onde-corpuscule (8)
- Il faut renoncer à la notion de trajectoire !
- Il faut accepter le caractère aléatoire !
- (probabiliste)
- Louis de Broglie a étendu cette dualité aux
particules de matière.
24
Dualité onde-corpuscule (9)
Quantification de lénergie Particule dans
une boite unidimensionnelle de longueur L
- énergie cinétique
- de Broglie
- condition de stationarité de londe
La quantification de lénergie ne provient que
des conditions aux limites !
25
Mécanique quantique (1)
- Mécanique classique
- Mécanique quantique
- Yi fonction donde qui décrit la particule.
- Ei énergie de létat de la particule décrit par
Yi - opérateur Hamiltonien
26
Mécanique quantique (2)
- Fonction donde Seul son carré à un sens
physique - dP Y2 dt probabilité de trouver la
particule dans le volume dt. - Elle doit être normée car la probabilité de
trouver lélectron dans tout lespace est
évidemment 1. - Cest la condition aux limites !!
27
Atomes Hydrogénoïdes (1)
- 1 seul électron H, He, Li2, U91,
- Énergie avec n entier positif !
- I 13,6 eV 0,5 u.a. ...
28
Atomes Hydrogénoïdes (2)
- Quest ce que lénergie dun atome ?
- énergie cinétique du noyau
- énergie cinétique de lélectron
- énergie potentielle attractive ény
Comme noyau beaucoup plus lourd quélectron ?
mouvements indépendants ? séparation des
variables (approximation de Born-Oppenheimer)
29
Atomes Hydrogénoïdes (3)
- Énergie avec n entier positif !
- Qd n 1 niveau le plus bas (fondamental)
- Qd n gt 1 niveau excité ( E lt 0)
- Si E ? 0 état ionisé