Diapositiva 1 - PowerPoint PPT Presentation
Title:
Diapositiva 1
Description:
11 Enlace Qu mico. Formulaci n F sica e Qu mica 4. ESO Exercicios: 1, 2, 3 1.-Escribe as f rmulas seguintes e pon o seu nome noutra nomenclatura: xido de ... – PowerPoint PPT presentation
Number of Views:72
Avg rating:3.0/5.0
Title: Diapositiva 1
1
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 1, 2, 3
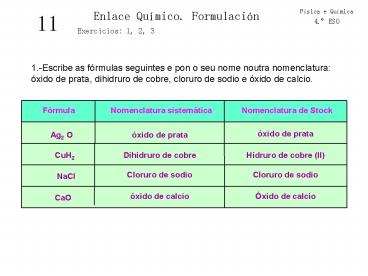
1.-Escribe as fórmulas seguintes e pon o seu nome
noutra nomenclatura óxido de prata, dihidruro de
cobre, cloruro de sodio e óxido de calcio.
Fórmula
Nomenclatura sistemática
Nomenclatura de Stock
óxido de prata
Ag2 O
óxido de prata
CuH2
Dihidruro de cobre
Hidruro de cobre (II)
Cloruro de sodio
Cloruro de sodio
NaCl
óxido de calcio
Óxido de calcio
CaO
2
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 1, 2, 3
2.-Explica cómo se forma o enlace iónico de cada
un dos compostos anteriores.
óxido de prata dihidruro de cobre cloruro de
sodio óxido de calcio
3.-Explica a formación de enlace das seguintes
sustancias SO, SO2 , e CO2.
SO son dous non metais que se unirán por enlace
covalente, compartindo electróns teñen 6
electróns de valencia e comparten dous SO SO2
O xofre comparte 4 e- con dous osíxenos
OSO CO2 igual que o anterior OCO
3
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 4,5
4.- Indica unha propiedade de cada unha das
seguintes substancias grafito, cloro, xofre e
diamante (cristal de carbono).
Grafito insoluble en auga Cloro Tª de fusión e
ebulición baixas. É un gas. Xofre insoluble en
auga. Diamante moi duro
5.-Escribe as formulas seguintes óxido de cloro
(V), amoníaco, bromuro de hidróxeno, teloruro de
hidróxeno
Cl2O5 NH3 HBr H2Te
Óxido de cloro (V) Amoníaco Bromuro de
hidróxeno Telururo de hidróxeno
4
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 6,7
6.-Formula e nomea de todas as formas posibles o
ácido sulfúrico, nitrito de sodio e sulfato de
magnesio.
Tetraoxosulfato (VI) de hidróxeno H2 S
O4 Dioxonitrato (III) de sodio Na N
O2 Tetraoxosulfato (VI) de magnesio Mg S O4
7.- Indica o proceso de formación dos sales
seguintes trioxocarbonato (IV) de ferro (ll), e
trioxonitrato(V) de potasio.
Trioxocarbonato (IV) de ferro (II) trioxocarbonat
o (IV) de hidróxeno H2CO3 CO3 ferro (II)
Fe2
FeCO3 Trioxonitrato (V) de potasio trioxonitrato
(V) de hidróxeno HNO3 NO3- potasio
K
KNO3
5
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 8, 9, 12
8.-Por que se utiliza o chumbo para fabricar
fusibles de seguridade nas instalacións
eléctricas?
Porque o chumbo ten unha temperatura de fusión
baixa, e tan pronto haxa unha subida de tensión,
fúndese abrindo o circuíto
9.- Que propiedades dos metais permiten usalos
para fabricar compoñentes de instalacións e
tendidos eléctricos?
A ductilidade e a conductividade eléctrica son as
propiedades que determinan o seu uso en
instalacións e tendidos eléctricos.
12.-Dos compostos seguintes, indica cáles terán
enlace iónico a) NaF c) HCIO e)
Cr2O3 b) SO2 d) KH f) HgO
Terán caracter iónico NaF, KH, Cr2O3 , HgO
6
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 13, 14
13.-Das substancias seguintes SO2, CaCl2, HCl,
H2SO4, Na2O, a) Indica o tipo de
enlace que se dá en cada unha delas b)
Escribe unha propiedade de cada unha. c)
Noméaas por algunha das nomenclaturas permitidas
pola IUPAC.
SO2 Enlace covalente dióxido de xofre óxido
de xofre(IV) CaCl2 Enlace iónico dicloruro
cálcico cloruro de calcio HCl Enlace
covalente cloruro de hidróxeno
H2SO4 Enlace covalente tetraoxosulfato (VI)
de hidróxeno Na2O Enlace iónico óxido de
disodio óxido de sodio
14.-Indica o proceso de formación do enlace no
óxido de magnesio.
MgO Mg ? 2 e- Mg O
2e- ? O
7
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 15
- 15.-Indica o modelo ou os modelos de enlace
coherentes con cada unha das seguintes
propiedades - Conducen a corrente eléctrica en estado líquido
- Son, en xeral, solubles en auga
- Son, en xeral, sólidos a temperatura ambiente.
- No son solubles en auga.
- Son moi duros.
- Teñen elevados puntos de fusión.
- Conducen a corrente eléctrica en estado sólido
- Son deformables.
e) Cristais covalentes e iónicos f) Cristais
covalentes e iónicos g) Metais h) Metais
- Iónicos e metálicos
- Iónicos
- Iónicos e metálicos e cristais covalentes
- Covalentes e metais
8
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 16, 17
16.-Como se unen entre si os átomos do ferro
para formarun bloque de este metal?
Ordenándo os catións metálicos nunha rede
cristalina na que se comparten electróns
17.-Debuxa os diagramas de Lewis que representan
o enlace covalente das seguintes substancias
a) Br2O c) SO3 e) CO2
b) HF d) O2 f) HClO
Br-O-Br
OCO
H-O-Cl
H-F
OO
9
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 18
18.-Nomea cada unha das substancias representadas
nas formulas da actividade anterior mediante
tódalas nomenclaturas permitidas.
Fórmula Sistemática Stock
Br2O Óxido de dibromo Óxido de bromo (I)
HF Fluoruro de hidróxeno Fluoruro de hidróxeno
SO3 Trióxido de xofre Óxido de xofre (VI)
O2 Osíxeno Osíxeno
CO2 Dióxido de carbono Óxido de carbono (IV)
HClO Monoxoclorato (I) de hidróxeno Monoxoclorato (I) de hidróxeno
10
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios19
19.-Completa os nomes dos compostos seguintes
Fórmula Sistemática Stock
HBr Bromuro de hidróxeno Bromuro de hidróxeno
CO2 Dióxido de carbono Óxido de carbono (IV)
NaOH Hidróxido de sodio Hidroxido de sodio
H2SO3 Trioxosulfato (IV) de hidróxeno Trioxosulfato (IV) de hidróxeno
KClO3 Trioxoclorato (V) de potasio Trioxoclorato (V) de potasio
K2O Monóxido de dipotasio Óxido de potasio
FeH2 Dihidruro de ferro Hidruro de ferro (II)
11
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 20
20.-Escribe as formulas seguintes
Fórmula Sistemática Stock
H2SO4 ácido sulfúrico Tetraoxosulfato (Vl) de hidróxeno
K2O Óxido de potasio
NaClO Hipoclorito de sodio Monoxoclorato (I) de sodio
MgH2 Hidruro de magnesio
MnO2 Dióxido de manganeso
Cl2O5 Óxido de cloro (V)
SO3 Trióxido de xofre
HNO3 Ácido nítrico Trioxonitrato (V) de hidróxeno
Al(OH)3 Hidróxido de aluminio
12
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 21
21.-Escribe as formulas seguintes
Fórmula Sistemática Stock
Mg H2 Hidruro de magnesio
Fe2O3 Óxido de ferro (lll)
Cl2O7 Oxido de cloro (Vll)
H2SO4 Tetraoxosulfato (Vl) de hidróxeno
H2SO4 ácido sulfúrico Tetraoxosulfato (Vl) de hidróxeno
Co2O3 Óxido de cobalto (lll)
CuSO3 Sulfito de cobre (ll) Trioxosulfato (IV) de cobre (II)
KClO3 Clorato de potasio Trioxoclorato (V) de potasio
HClO4 Ácido perclórico Tetraoxoclorato (VII) de hidróxeno
13
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 22
22.-Nomea con outra nomenclatura distinta da
empregada tódolos compostos das actividades 20 e
21
Fórmula Sistemática Stock
H2SO4 ácido sulfúrico Tetraoxosulfato (Vl) de hidróxeno
K2O Óxido de dipotasio Óxido de potasio
NaClO Hipoclorito de sodio Monoxoclorato (I) de sodio
MgH2 Dihidruro de magnesio Hidruro de magnesio
MnO2 Dióxido de manganeso Óxido de manganeso (IV)
Cl2O5 Pentóxido de dicloro Óxido de cloro (V)
SO3 Trióxido de xofre Óxido de xofre (VI)
HNO3 Ácido nítrico Trioxonitrato (V) de hidróxeno
AL(OH)3 Trihidróxido de aluminio Hidróxido de aluminio
14
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 22
22.-Nomea con outra nomenclatura distinta da
empregada tódolos compostos das actividades 20 e
21
Fórmula Sistemática Stock
Mg H2 Dihidruro de magnesio Hidruro de magnesio
Fe2O3 Trióxido de diferro Óxido de ferro (lll)
Cl2O7 Heptóxido de dicloro Oxido de cloro (Vll)
H2SO4 Tetraoxosulfato (Vl) de hidróxeno Tetraoxosulfato (Vl) de hidróxeno
H2SO4 ácido sulfúrico Tetraoxosulfato (Vl) de hidróxeno
Co2O3 Trióxido de dicobalto Óxido de cobalto (lll)
CuSO3 Sulfito de cobre (ll) Trioxosulfato (IV) de cobre (II)
KClO3 Clorato de potasio Trioxoclorato (V) de potasio
HClO4 Ácido perclórico Tetraoxoclorato (VII) de hidróxeno
15
11
Enlace Químico. Formulación
Física e Química 4.º ESO
Exercicios 23
23.-Unha sustancia pura é sólida a temperatura
ambiente, presenta un elevado punto de fusión e
conduce a corrente eléctrica. Indica o tipo de
enlace que une os seus átomos.
Ten que ser un enlace metálico, por ser conductor
en estado sólido