1. dia - PowerPoint PPT Presentation
Title:
1. dia
Description:
Title: 1. dia Author: seram Last modified by: ELTE Created Date: 9/26/2004 10:10:41 AM Document presentation format: Diavet t s a k perny re (4:3 oldalar ny) – PowerPoint PPT presentation
Number of Views:172
Avg rating:3.0/5.0
Title: 1. dia
1
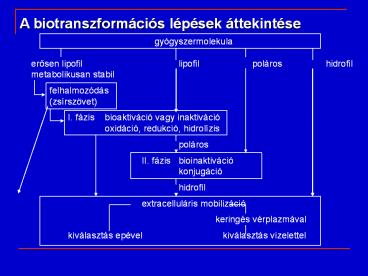
A biotranszformációs lépések áttekintése
gyógyszermolekula erosen
lipofil lipofil poláros hidrofil metabolikusan
stabil felhalmozódás (zsírszövet) I.
fázis bioaktiváció vagy inaktiváció oxidáció,
redukció, hidrolízis poláros II.
fázis bioinaktiváció konjugáció hidrofi
l extracelluláris mobilizáció keringés
vérplazmával kiválasztás epével
kiválasztás vizelettel
2
A biotranszformációs lépések áttekintése
gyógyszermolekula erosen
lipofil lipofil poláros hidrofil metabolikusan
stabil felhalmozódás (zsírszövet) I.
fázis bioaktiváció vagy inaktiváció oxidáció,
redukció, hidrolízis poláros II.
fázis bioinaktiváció konjugáció hidrofi
l extracelluláris mobilizáció keringés
vérplazmával kiválasztás epével
kiválasztás vizelettel
3
A biotranszformáció II fázisának reakciói
I. Konjugációs reakciók Exogén szubsztrát funkciós csoportja Kofaktor Enzim A reakció helye
Glükuronsavas konjugáció -OH, -COOH, -NH2, -NH, -SH, -CH UDPGA Glükuronil transzferáz (GT) Sima endoplazmás retikulum
Szulfát konjugáció aromás-OH/NH2 -COOH PAPS Szulfotranszferáz Citoszol
Glicin konjugáció aromás-NH2, -COOH KoenzimA Glicin Aminosav-aciltranszferáz Mitokondrium
Acetilálás aromás/alifás-NH2, hidrazinok, -SO2, NH2 Acetil koenzimA N-, O-acetil transzferáz Citoszol (van mikroszómális is)
Metilálás aromás-OH, NH2, NH -SH Adenozil-S- metionin Metiltranszferáz Citoszol (van mikroszómális is)
Glutation konjugáció epoxid, szerves haloid Redukált glutation Glutation transzferáz Citoszol (van mikroszómális is)
II. Nem konjugációs reakciók enzimjei epoxid hidrolázok, glioxalázok, karboxilészterázok II. Nem konjugációs reakciók enzimjei epoxid hidrolázok, glioxalázok, karboxilészterázok II. Nem konjugációs reakciók enzimjei epoxid hidrolázok, glioxalázok, karboxilészterázok II. Nem konjugációs reakciók enzimjei epoxid hidrolázok, glioxalázok, karboxilészterázok II. Nem konjugációs reakciók enzimjei epoxid hidrolázok, glioxalázok, karboxilészterázok
4
A kevert funkciójú oxidáz rendszer
elhelyezkedése a sima endoplazmás retikulumban
kofaktorok xenobiotikum
fp1, fp2 flavoproteinek b5 citokróm b5
5
A glükuronsav uridin difoszfát szintézise (nagy
energiatartalmú molekula)
6
A fenol glükuronsavas konjugációja
7
A glükuronsavas konjugáció jellemzoi
- Gyors (endoplazmatikus retikulumban, MFO
komplexhez kapcsolódva) - Gyakori (a gyógyszer molekulák jelentos részénél
végbemegy) - Nem mutat telítodést
- Egy gyógyszer molekulára több glükuronid csoport
is kerülhet (több poláros csoport esetén) - OH csoporton, vagy NH2 csoporton (N-glükuronid)
8
Morfin glükuronidjai
- Morfin-6-glükuronid- hatékonyabb, mint az eredeti
molekula - Morfin-3-glükuronid-hatástalan
9
A fenol átalakulása fenilszulfáttá
szulfuriláz SO42- ATP APS PPi
(pirofoszfát)
(adenozin-foszfoszulfát ,
pirofoszfát) APS foszfokináz APS
ATP PAPS ADP
(foszfo-adenozin-foszfo-szulfá
t)
10
Szulfát konjugáció jellemzoi
- Bizonyos szubsztrát-specificitás (fenolok,
alkoholok, szteroidok) - Az exogén szubsztrátok poláros csoportjai aromás
OH, aromás amin, szerves sav - Telítheto (a szulfát készlet véges)
- A 2. leggyakoribb II.fázis reakció
- Általában a citoszolban zajlik
- A szulfotranszferáz enzimnek (ST) sok izozimje
van
11
Aminosav konjugáció
- Leggyakrabban glicin konjugáció, de elofordul más
aminosavval történo konjugáció is - Nem az endogén szubsztrát (glicin) hanem a
kofaktor koenzimA kerül aktivált állapotba - Mitokondriumokban zajlik (Aminosav
acil-transzferázok)
12
Acetilálás
- Funkciós csoportok alifás, aromás aminok,
amidok, hidrazinok, szulfamidok - EnzimekN-acetil transzferáz, O-acetil
transzferáz - A reakció helyszíne citoszol
13
Metilálás
- Funkciós csoportok hidroxil, amino csoport
- Kofaktoradenozil-S-metionin (nagy energiájú
metil donor) - Enzimek metil-transzferázok
- A reakció helyszíne citoszol, endoplazmás
retikulum
14
Glutation konjugáció
- glutation tripeptid, gamma-glutamil-ciszteinil-gl
icin, GS - Veszélyes molekulákat alakít át merkaptúrsavvá
(kevés gyógyszermolekula konjugálódik
glutationnal)
15
Glutation konjugáció merkaptursav képzodése
16
Epoxid átalakulása merkaptursavvá
glutation konjugációval
17
A II. fázis nem konjugációs reakciói
- Epoxid hidrolázok
- Glioxalázok
- Karboxilészterázok által
katalizált reakciók
18
Epoxidok eliminációja epoxid hidroláz enzim
segítségével
- Pl. Brómbenzolból brómbenzol 3,4 epoxid jön létre
(I.fázis), ami epoxid hidroláz enzim segítségével
brómbenzol 3,4 hidrodiollá alakul. A reakció elso
lépéseként az enzim aktivál (deprotonál) egy
vízmolekulát.
19
- A biotranszformáció II. fázisa
- Általában bioinaktivációt jelent
- Kivételes esetben aktiváció is történhetelekrofi
l gyökök keletkezhetnek.
20
Karbónium és nitrénium ion képzodése
benzilalkohol és hidroxámsav szulfátkonjugátumábó
l
21
Thiiránium ion keletkezése dibróm etán
glutationos konjugációja után
22
Aromás aminok inaktivációja a májban és
reaktivációja a hugyhólyagban
23
Tiol képzodése cisztein glutation konjugátumából
24
Egy molekula metabolizmusának vizsgálata
- Rádioaktív jelöléssel ellátott molekulával
végzett in vivo állatkísérletek - In vitro kísérletek
25
A dimethachlor metabolikus átalakulása (18
azonosított metabolit)
26
A biotranszformációt befolyásoló tényezok
- Faj
- Fajon belüli genetikai különbségek
- Életkor
- Élettani állapot
- Külso tényezok (egyéb gyógyszerek, élelmiszerek,
élvezeti cikkek)
27
A fenol glükuronsavas és szulfátos
konjugációjának aránya néhány fajnál
Glükuronid konjugáció () Szulfát konjugáció ()
Macska 0 87
Ember 23 71
Patkány 25 68
Nyúl 46 45
Disznó 100 0
28
Amfetamin biotranszformációja nyúl,
patkány tengerimalac és kutya esetében
29
A biotranszformáció I. fázisának reakciói
az életkor függvényében
30
Születés elotti hatások
- A thalidomid története
- 1953 szintézis, Chemie Grünenthal
- 1957. forgalmazás kezdete
31
Thalidomide S nyugtató hatású
R torzkelto (teratogén)
32
Thalidomide babies
33
(No Transcript)
34
A tragédia okai
- Faji különbségek
- Életkor okozta különbségek
35
Néhány példa a biotranszformációs
folyamatokat befolyásoló külso tényezokre
Környezeti tényezok Inszekticidek, herbicidek, nehézfémek, ipari szennyezo anyagok
Étrendi tényezok Indolok, dohánytermékek, marihuána termékek, alkoholfogyasztás, pirolízis termékek, a táplálék egyes alkotórészei (nyomelemek, ásványi anyagok, vitaminok, fehérjék, lipidek, szénhidrátok
36
Néhány bifenil molekulasúlya és kiválasztási útja
patkányban
Nefron
Kiválasztás útja () Kiválasztás útja ()
Anyag Molekulatömeg Vese Fécesz
Bifenil 154 80 20
4-monoklórbifenil 188 50 50
4,4-diklórbifenil 223 34 66
2,4,5,2,5-pentaklórbifenil 326 11 89
2,3,6,2,3,6-hexaklórbifenil 361 1 99
Referencia H. B. Mattheus in Introduction to
Biochemical Toxicology (1960)
37
Enterohepatikus körforgás